食肉用語の解説ミオシン
ミオシンは骨格筋や食肉の主要なタンパク質の一つで、1868年にドイツのキューネによって発見された。その後、1939年にソビエトのエンゲルハルト夫妻によって、ミオシンがATP分解酵素であることが突き止められたことを発端に、セントジェルジとその同胞らによって、ミオシンが筋収縮の主要な役割を果たしていることが明らかにされた。ミオシンは、骨格筋だけでなく他の器官や組織においてもさまざまな構造類似体が存在しているが、最初に骨格筋で発見されたことから、一般的に“ミオシン”とする場合は骨格筋のミオシンを指す。
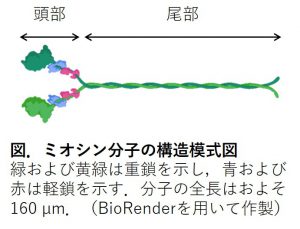
ミオシンの単分子は、2本の重鎖と4本の軽鎖からなる六量体の構成をとり、その分子量はおよそ50万である。重鎖はそれぞれN末端側で球状の構造をとるが、C末端側では棒状の構造をとる。この棒状部分はほぼ全域にわたってαヘリックス構造であり、2本の重鎖はこの部分で絡まりあい、coiled-coil構造をとっている。つまり、ミオシンは、二つの頭をもったオタマジャクシのような分子構造となっており、N末端側を頭部、C末端側を尾部と称する場合もある。骨格筋においてミオシンは、300近い分子が会合し、“太いフィラメント”として、筋原線維内に存在している。
ミオシンの主な生理機能は以下の3つである。(1)ATPを分解する、(2)アクチンと結合する、(3)“太いフィラメント”を形成する。このうち(1)と(2)はミオシンの頭部領域、(3)は尾部領域に、それぞれ作用部位があることがわかっている。また、ミオシンは、生理的塩濃度以下の水溶液では重合体を形成するため溶解せず、高塩濃度溶液にのみ溶解する塩溶性のタンパク質とされている。
食肉加工においてもミオシンは重要な役割を果たしている。ミオシンは加熱するとゲルを形成することがわかっており、この機能によって食肉製品は保水性を発現することができる。食肉製品の保水性・結着性は、その品質を左右する重要な因子であるため、ミオシンのゲル形成機構の解明は食肉科学分野において重要な課題であった。当研究会の元会長でもある安井らのグループによって、その大よそは解明さている。この詳細については、会誌「食肉の科学」(または前身の「肉の科学」)にも掲載されているので、そちらを参照されたい1-3)。
1)鮫島邦彦・安井勉, 肉の科学, 21 (1), 1-24 (1980)
2)鮫島邦彦, 食肉の科学, 46 (2), 161-168 (2005)
3)石下真人, 食肉の科学, 57 (2), 163-168 (2016)
(北海道大学 早川徹)


